Project Description
Enfermedad potencialmente grave, la fiebre amarilla es causada por virus. La mayoría de las personas infectadas tienen pocos síntomas o no los presentan. Sin embargo, cuando la enfermedad se manifiesta, tiene un alto grado de letalidad.
Gravedad de la fiebre amarilla:
La letalidad puede variar del 30% al 60%.
Manifestaciones
Comienzan repentinamente e incluyen síntomas como:
- fiebre alta
- escalofríos
- cansancio
- dolor de cabeza
- dolor muscular
- náuseas y vómitos durante unos tres días
Después de un breve período (cerca de dos días), la afección puede evolucionar para cura o para la forma más grave. Cuando eso ocurre es marcada por:
- insuficiencias hepáticas y renil
- ictericia (ojos y piel amarillento)
- manifestaciones hemorrágicas
- cansancio severo
Transmisión
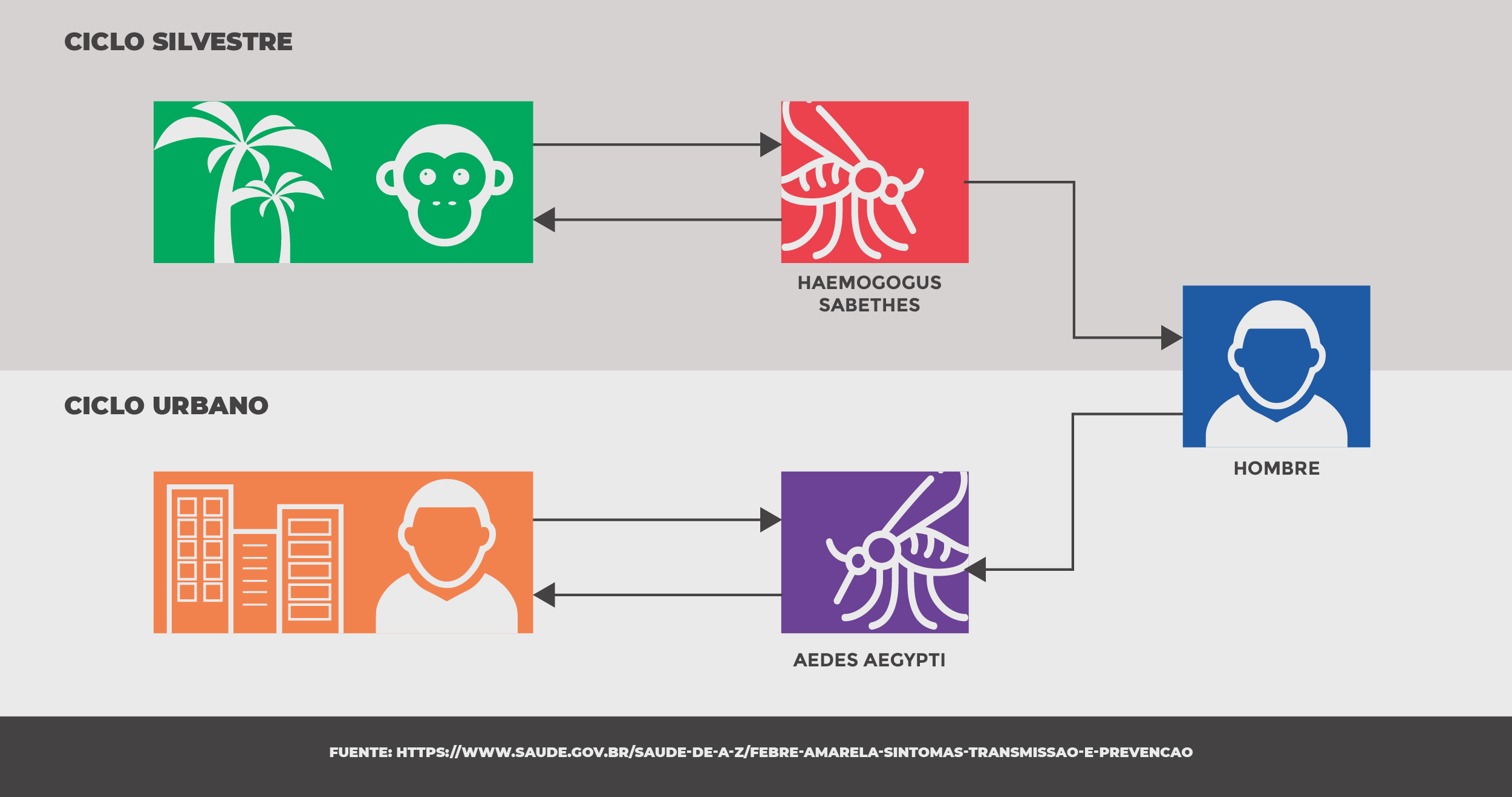
Actualmente, la transmisión silvestre (en áreas forestales) es la más común. Ocurre cuando el mosquito de los géneros Haemagogus muerde a un mono* infectado y, después, comienza a infectar a los seres humanos. En las zonas urbanas, la fiebre amarilla puede ser transmitida principalmente por el mosquito Aedes aegypti ─ el mismo agente transmisor del dengue ─ después de picar una persona infectada.
Ciclos de transmisión de virus:
Los movimientos de población y el aumento de los viajes alrededor del mundo, sumados al número de personas susceptibles, plantean riesgos de reintroducción de la fiebre amarilla en grandes áreas urbanas ubicadas en regiones tropicales y subtropicales que están infestadas de mosquitos capaces de transmitir el virus.
* Los monos no transmiten el virus de la fiebre amarilla a los humanos, ellos son nuestros aliados. La muerte de estos animales a causa de la enfermedad es una señal de alerta.
Prevención
La vacunación es la forma más segura y efectiva de prevenir la transmisión y los brotes de fiebre amarilla.
Vacunas
Todas las vacunas contra la fiebre amarilla comercializadas actualmente se elaboran a partir de virus vivos atenuados, cultivados en huevo de pollo.
Son vacunas precalificadas por la OMS:
- Bio-Manguinhos/Fiocruz
- Sanofi Pasteur AS (Stamaril®)
- Institut Pasteur de Dakar
Indicaciones
La vacunación está indicada a partir de los 9 meses de edad para todos que viven o viajan por cualquier zona en la que se hayan notificado casos, a menos que pertenezcan a alguno de los grupos de personas en las que la vacuna esté contraindicada.
Atención especial a los viajeros
Toda persona mayor de 9 meses que viaje hacia las zonas de riesgo o regrese de ellas debe estar vacunada, a menos que pertenezca a alguno de los grupos de personas en las que la vacuna esté contraindicada.
Los viajeros originarios de regiones endémicas pueden tener que presentar, en el país de destino, el Certificado Internacional de Vacunación y Profilaxis (CIVP) con el registro de dosis aplicada al menos diez días antes del viaje.
Cuando hay una contradicción para la vacunación contra la fiebre amarilla, el médico puede expedir el certificado con la justificación de la exención.
Eficacia
La vacunación a gran escala contra la fiebre amarilla ha sido extremadamente eficaz con perfil estimado por encima del 95%. Prueba de la efectividad es que en los lugares donde han cesado las campañas de vacunación masiva y no se ha mantenido la cobertura de vacunación (número ideal de personas vacunadas), la enfermedad ha vuelto a aparecer y producido grandes brotes.
Seguridad
Todas las vacunas pre calificadas por la OMS para la prevención de la fiebre amarilla tienen un gran y similar perfil de seguridad y también de eficiencia, y pueden ser utilizadas de forma intercambiable en los programas de inmunización.
Efectos adversos
Las manifestaciones generales como fiebre, dolor de cabeza y músculo son los eventos más frecuentes y ocurren en aproximadamente el 4% de las personas que están vacunadas la primera vez y menos del 2% en las segundas dosis.
Las manifestaciones locales, como el dolor en el área de aplicación, se producen en el 4% de los adultos vacunados y un poco menos en niños pequeños. El dolor dura uno o dos días, en forma leve o moderada.
Las reacciones alérgicas como erupciones cutáneas, urticaria y asma a menudo ocurren de un caso a 130.000 a 250.000 vacunados.
Efectos adversos graves y muy raros
reacciones anafilácticas o de hipersensibilidad graves inmediatas;
enfermedades neurológicas asociadas a la vacuna;
enfermedades viscerotrópicas asociadas a la vacuna.
En Brasil, donde se recomienda la vacunación desde hace décadas, la ocurrencia de estos graves acontecimientos fue:
de 0,42 caso por cada 100 mil vacunados, entre 2007 y 2012;
de 0,023 caso de anafilaxia en la proporción de cien mil dosis aplicadas entre 1999 y 2009;
0,2 caso de enfermedad neurológica en 100.000 vacunados, entre 2007 y 2012, especialmente cuando se trataba de una primera dosis y en los ancianos;
en el mismo período, ocurrió apenas 0,04 caso de la enfermedad de los órganos, llamada viscerotrópica, en 100 mil vacunados.
Contraindicaciones
- Niños menores de 6 meses de edad.
- Personas infectados por el VIH, sintomáticos y con inmunosupresión grave probados por un examen de laboratorio.
- Personas con inmunodepresión grave debido a enfermedades o al uso de medicamentos.
- Personas sometidas a trasplante de órganos.
- Personas con antecedentes de enfermedades del timo (miastenia grave, timoma, casos de ausencia de timo o extirpación quirúrgica).
- Personas que han tenido enfermedad neurológica desmielinizante dentro de las seis semanas siguientes a la aplicación previa de la dosis de la vacuna.
- Personas con antecedentes de reacción anafiláctica relacionada con sustancias presentes en la vacuna (huevo de pollo y sus derivados, gelatina bovina u otros).
- Mujeres amamantando a los niños menores de 6 meses. Si no se puede evitar la vacunación, se debe interrumpir la lactancia durante 10 días. Se debe consultar al pediatra para obtener más informaciones / orientaciones.
- En principio, las mujeres embarazadas no deben recibir esta vacuna, pero la administración debe analizarse en función del grado de riesgo ─ por ejemplo: cuando ella vive en un lugar con brotes de la enfermedad.
Precauciones
- En caso de fiebre se recomienda posponer la vacunación hasta la mejora;
- Individuos de 60 años o más no vacunados previamente: aunque raros, se describe un mayor riesgo de eventos adversos graves en la primera vacunación en este grupo de edad;
- Personas que viven con VIH/SIDA, asintomáticas y que presentan LT-CD4 a 350 células/mm3. Se puede utilizar la última prueba LT-CD4 (independientemente de la fecha), siempre que la carga viral actual (menos de seis meses) permanezca indetectable;
- Personas después de la finalización del tratamiento de quimioterapia (venoso u oral) y sin un nuevo ciclo: administrar la vacuna tres meses después del final de la quimioterapia;
- Personas que usaron células B y fludarabina deben esperar con seis meses de diferencia;
- Personas sometidas a trasplante de células madre hematopoyéticas: puede recibir esta vacuna a partir de los 24 meses posteriores al trasplante si no hay injerto contra enfermedad del huésped y/o recaída de la enfermedad de la piel inferior y/o el uso inmunosupresor;
- Síndrome mieloproliferativo crónico: la vacuna pude ser administrada si el estándar de laboratorio es estable y con neutrófilos por encima de 1500 cels/mm3;
- Síndrome linfoproliferativo: la vacuna puede ser administrada apenas tres meses después del final de la quimioterapia (excepto en el caso de uso de medicamentos anti-B de células B, cuando el intervalo debe ser de seis meses);
- La administración de la vacuna en personas con lupus eritematoso sistémico u otras enfermedades autoinmunes debe ser evaluada cuidadosamente, ya que puede haber inmunosupresión.
Enfermedades hematológicas:
- hemofilia y enfermedades hemorrágicas hereditarias: la vacuna debe ser administrada de acuerdo con la orientación del Calendario Nacional de Vacunación. Se recomienda utilizar compresas frías antes y después de la aplicación de la vacuna;
- Enfermedad de células falciformes:
- sin el uso de hidroxiurea – la vacuna puede ser administrada de acuerdo con el Calendario Nacional de Vacunación;
- si en uso de hidroxiurea: la vacuna solo puede ser administrada si el neutrófilo cuenta por encima de 1500 cels/mm3.
Composición
Todas las vacunas contra la fiebre amarilla comercializadas actualmente se elaboran a partir de virus vivos atenuados, cultivados en huevo de pollo y, dependiendo del fabricante, pueden tener en la formulación la presencia de:
- gelatina bovina;
- eritromicina;
- canamicina;
- clorhidrato de L-histidina;
- L-alanina;
- cloruro de sodio y agua para inyección;
- lactosa;
- sorbitol;
- clorhidrato de L-histidina;
- L-alanina;
- solución salina.